治疗不良反应(adverse reaction)应包括药物治疗、手术治疗及其他治疗的各种不良反应在内。现以药物治疗不良反应为例。
(一)药物不良反应的严重性
表6-7 英国医药安全委员会报告药物不良反应的报告数和死亡百分比(1964.1~1976.6)
| 药 物 | 报 告 数 | 死亡(%) |
| 氟 烷 | 380 | 42 |
| 羟基保泰松 | 709 | 23 |
| 保泰松 | 1364 | 26 |
| 阿司匹林 | 410 | 26 |
| 氯丙嗪 | 584 | 20 |
| 三氟丙嗪 | 306 | 15 |
| 苯巴比妥 | 353 | 14 |
| 氯氮卓 | 567 | 13 |
| 丙咪嗪 | 446 | 12 |
| 地西泮 |
(式6-7)
分式中n=治疗人数,p=人群中抑郁症的发生率,e为自然对数底=2.7183。
40人中出现该抑郁症1人的概率
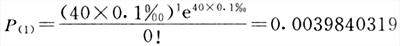
还可计算在40人中出现抑郁症2,3,4…40人的概率,这些概率更小了。
为计算方便起见,可计算1例也不出现的概率:
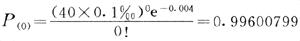
然后以1-0.99600799=0.00399201,此概率代表出现1例及多例的总概率。这总概率<0.005,说明这一例在不吃药的人群出现的概率太小,假设被拒绝。因而可以认为40个服药人中出现一例抑郁症与服药有关,应停止临床应用该药物。
2.干预试验法 干预试验可判断药物与不良反应的关系。
如反应停(商品名Grippex)有安眠和镇静作用,常为孕妇所使用。在联邦德国,从1959年开始在市场销售,1960年销售量迅速上升。1960年底和1961年初出生短肢畸形病例数亦随之上升。两条曲线相隔3个季度,故反应停销售量曲线正与这些病例的母亲怀孕初期相吻合。1961年12月对反应停进行干预,从联邦德国市场撤消,反应停停止出售后,1962年下半年以后出生的儿童便很少发生这种畸形。说明此不良反应是反应停所致。见图6-6。
(四)药物不良反应的监测
药物不良反应已成为一个全球性的问题。
我国卫生部根据《中华人民共和国药品管理法》第24条,25条规定:为保证人民用药安全制定了“药品不良反应监测报告制度”。
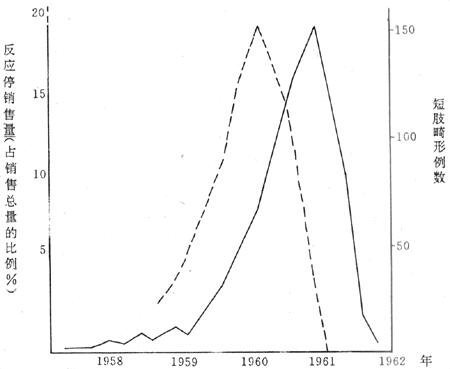
图6-6 联邦德国反应停销售总量(虚线)与短肢畸形病例数(实线)
的时间分布(Davis and Dobbling.1974)
监测的目的在于及时发现上市后药物未预料到的严重不良反应。确立已知或新发现不良反应的情况,对药物不良反应进行流行病学调查,以及研究其机制和后果等。
监测方法:
(1)医院为中心的监测系统:可以按照划区或医疗分工,与卫生院、诊所、保健站等形成监测网,省、地(市)医院内专设流行病学(或临床流行病学)科承担药物监测,包括药物不良反应的登记、分析和进行专题研究,为国家药政部门提供信息和药物生产使用的依据。美国波士顿1965年开始的药物监测协作计划(BCDSP),是以医院为中心进行药物监测的,具有代表性的项目。
上海市进行药物监测的试点工作,选择9所医院的部分病房,对1200名住院病人进行为期3个月至1年的药物不良反应监测。如上海市部分医院的内科和儿科,药物不良反应的发生率分别为39%和12.9%。
(2)义务报告系统:英国自1964年起实行药物不良反应报告制度,即黄卡系统(yellow card system)。黄卡是随药附送的一种预付邮资和写明地址的明信卡,所以来源极为广泛,可来自医生,亦可来自患者,有代表性的耗资低。该系统对深入研究和观察药物不良反应起着“信号”作用。如ibutenac(抗炎止痛药)在投入市场后不久,英国药物安全委员会就收到40例肝损害的报告,决定立即终止销售。
(3)生命统计:药物不良反应的信息可以来自国家的生命统计,可在死亡报告中单列药物不良反应一项原因作统计分析。此法虽然简便经济,但是不能得到详尽的资料。
(4)记录连结:许多国家建立了记录连结(record linkage)体系,记录每个人出生后到死亡的重要健康和疾病问题,贮存在计算机内,对于研究药物或遗传同环境因素的致病作用是非常有用的,可以选择适当的对照,甚至配比的对照者进行病例对照研究。例如孕期子宫照射增加子女发生白血病的危险性,孕期使用已烯雌酚致女儿青春期阴道腺癌的研究,都是应用记录连结完成的。
(5)加强药政管理,认真贯彻执行《中华人民共和国药品管理法》,严格新药、新制剂的审批及作好老药复审再评价工作,充分应用立法权减少药品所造成的生命损失,以法律武器来保障人民的用药安全。
全部讨论(0)
请在登录后参与讨论...